Một số bác sĩ tại TP.HCM cảm thấy lo lắng vì nhiều F0 đang phải mua thuốc kháng virus điều trị Covid-19 với giá đắt đỏ nhưng không đảm bảo chất lượng.
Ngày 29/12/2021, Chính phủ Lào chính thức cho phép kinh doanh thương mại thuốc Molnupiravir (thuốc kháng virus điều trị Covid-19). Thuốc do Doanh nghiệp dược phẩm nhà nước Lào số 3 sản xuất, đóng trong bao bì có tên gọi Molacovir, lọ 40 viên.
Thông tin tích cực này ở nước bạn khiến người dân TP.HCM có phần sốt ruột. Giám đốc Sở Y tế TP.HCM Tăng Chí Thượng trong phiên chất vấn kỳ họp thứ 4, Hội đồng nhân dân TP.HCM khóa X từng chia sẻ, trong tương lai rất gần, người dân có thể mua thuốc điều trị Covid-19 tại nhà thuốc tây.

Thuốc Molnupiravir được cấp phát cho người dân trong chương trình thử nghiệm lâm sàng của Bộ Y tế.
Đến nay, thuốc Molnupiravir vẫn chưa được cấp phép lưu hành tại Việt Nam. Việc cấp thuốc cho F0 tại nhà cũng chưa đủ so với nhu cầu. TP.HCM đang ưu tiên tối đa Molnupiravir cho F0 thuộc nhóm nguy cơ (kể cả không triệu chứng) nhằm bảo vệ người bệnh yếu thế.
Trong khi đó, khảo sát các hội nhóm trên mạng xã hội, thuốc kháng virus điều trị Covid-19 đang được rao bán có giá từ trên 2,5 triệu đồng đến 3,6 triệu đồng/hộp. Người bán khẳng định, thuốc nhập từ Ấn Độ có tên thương mại là Molaz, đủ dùng trong 5 ngày.
“Một hộp em cũng giao tận nơi, không mất t.iền ship. Chị nhận thuốc và kiểm tra tại chỗ, nếu ưng mới trả t.iền”, một tài khoản tên N.N trên Facebook tư vấn.
Cũng chính loại thuốc này, hồi tháng 11/2021, được công khai giá 9,5 triệu đồng/hộp. Đó là thời điểm nhiều phường, xã tại TP.HCM tạm hết thuốc Molnupiravir cấp phát cho người dân trong khi số F0 tăng cao.
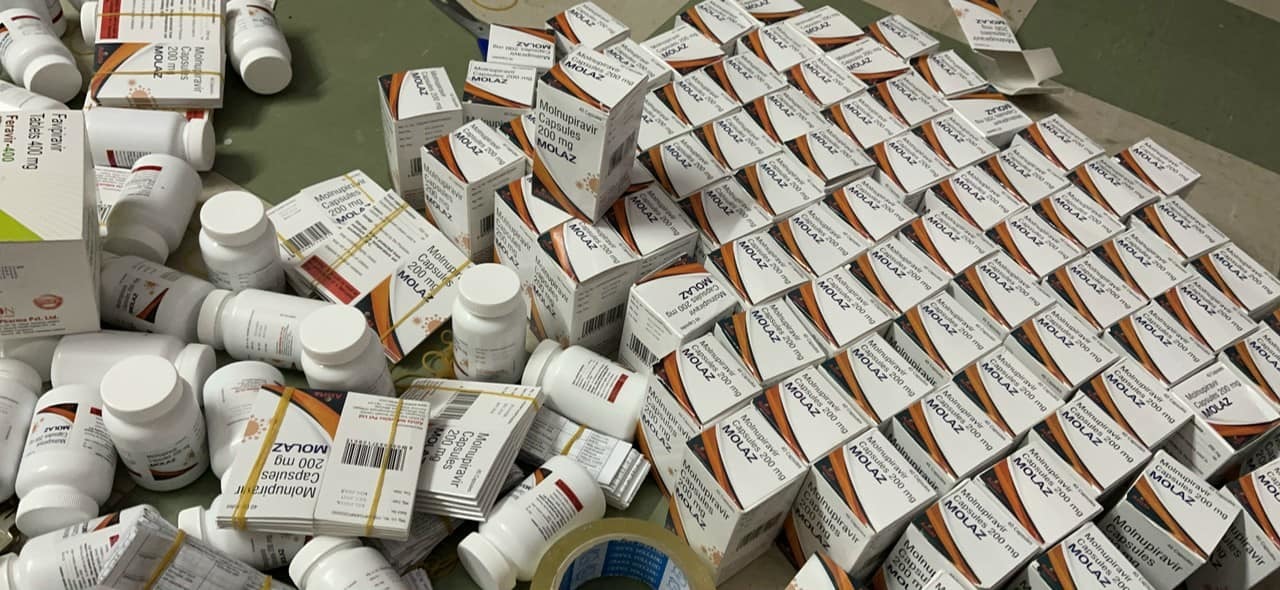
Loại thuốc được báo giá 2,5 đến 3,6 triệu đồng/hộp.
PGS. TS. BS. Vũ Minh Phúc, Giảng viên Đại học Y dược TP.HCM, chia sẻ, chị và nhiều bác sĩ tham gia tư vấn F0 cảm thấy sốt ruột khi một số bệnh nhân phải tìm mua thuốc với giá đắt đỏ. Buôn bán thuốc Molnupiravir hiện nay là vi phạm pháp luật và không đảm bảo chất lượng.
“Thuốc Molnupiravir trong chương trình thử nghiệm lâm sàng đã chứng minh hiệu quả tốt trong thời gian qua. Nếu chúng ta không kịp thời có các biện pháp để cấp phép lưu hành, sản xuất, cung ứng thuốc cho F0 điều trị thì rất tội cho người dân”, PGS Phúc chia sẻ.
Trong khi đó, bác sĩ Trương Hữu Khanh, Phó Chủ tịch hội truyền nhiễm TP.HCM cho rằng, vắc xin hiện vẫn là giải pháp chủ động hiệu quả trước Covid-19, kể cả với biến chủng Omicron. Người bệnh nhẹ tự theo dõi tại nhà, các bệnh viện tập trung điều trị cho ca nặng và người thuộc nhóm nguy cơ.
“Tuy nhiên, hiệu quả này đạt được khi F0 tại nhà tiếp cận được đủ thuốc kháng virus để không chuyển nặng và không phải nhập viện”, ông chia sẻ.
Hiện nay, thuốc Molnupiravir vẫn đang là thuốc sử dụng có kiểm soát, phải có cam kết, ký nhận theo quy định. Bác sĩ Khanh cho rằng, ngành y tế có thể giảm thủ tục để người dân nhận thuốc dễ hơn nếu đủ nguồn cấp miễn phí.
Giải pháp thứ 2, lý tưởng hơn, là các bộ ngành đẩy mạnh tiến độ cấp phép, sản xuất và cho phép kinh doanh thuốc Molnupiaravir hợp pháp. “Người dân mua thuốc tại cửa hàng, có quản lý của nhà nước thì không còn cảnh mua thuốc lậu với giá hàng triệu đồng nữa”, bác sĩ Khanh bày tỏ quan điểm.
Cũng theo bác sĩ Khanh, nếu người bệnh được hướng dẫn cụ thể, kỹ lưỡng về cách thức sử dụng, đối tượng, liều dùng… sẽ kiểm soát được tác dụng phụ của thuốc. Còn hiện nay, các bác sĩ vẫn khuyến cáo người dân phải chấp hành đúng các quy định trong cách ly điều trị tại nhà và sử dụng thuốc điều trị Covid-19.
Đến nay, Bộ Y tế đã phân bổ 300.000 liều thuốc Molnupiravir cho các địa phương đang triển khai Chương trình sử dụng thuốc có kiểm soát cho F0 triệu chứng nhẹ.

Người dân mong mỏi sớm được mua thuốc điều trị Covid-19 tại nhà thuốc.
Kết quả báo cáo giữa kỳ cho thấy, thuốc có tính an toàn cao, dung nạp tốt, hiệu quả rõ rệt về giảm tải lượng virus, giảm lây lan, giảm chuyển nặng, rút ngắn thời gian điều trị. Trong đó, tỷ lệ chuyển nặng rất thấp từ 0,02%-0,06% và không có ca nào dẫn đến t.ử v.ong.
Từ ngày 30/12/2021, Nghị quyết số 12/2021/UBTVQH 15 về cho phép thực hiện một số cơ chế, chính sách trong lĩnh vực y tế để phục vụ công tác phòng, chống dịch Covid-19 bắt đầu có hiệu lực. Trong đó, quy định nội dung về việc quản lý thuốc, nguyên liệu làm thuốc trong bối cảnh dịch Covid-19.
Cụ thể, đối với các thuốc mới có chỉ định điều trị Covid-19 sản xuất trong nước, nếu có cùng dạng bào chế, đường dùng, hàm lượng với thuốc đã được một trong những cơ quan quản lý dược nghiêm ngặt (SRA) cấp phép thì Việt Nam cho phép miễn nộp hồ sơ nghiên cứu lâm sàng trong hồ sơ đề nghị cấp giấy đăng ký lưu hành.
Đây được xem là chìa khóa tháo gỡ điểm nghẽn trong sản xuất thuốc điều trị Covid-19 tại Việt Nam. Theo Bộ Y tế, hiện có 10 công ty dược trong nước đề nghị cấp phép sản xuất Molnupiravir, nguyên liệu sản xuất cũng đã nhập khẩu về.
Bộ Y tế đã phân bổ 300.000 liều thuốc Molnupiravir điều trị bệnh nhân Covid- triệu chứng nhẹ
Dựa trên hiệu quả trong điều trị Covid-19 thể nhẹ của thuốc Molnupiravir, Bộ Y tế sẽ tiếp tục triển khai Chương trình sử dụng thuốc Molnupiravir để hạn chế các ca bệnh tiến triển nặng.
Ngày 18/12, Bộ Y tế đã phân bổ 300.000 liều thuốc Molnupiravir cho các địa phương đang triển khai Chương trình sử dụng thuốc có kiểm soát Molnupiravir cho các trường hợp mắc Covid-19 thể nhẹ tại cộng đồng.
Chương trình này được triển khai dựa trên cơ sở những kết quả nghiên cứu thử nghiệm lâm sàng thuốc Molnupiravir trong điều trị Covid-19 đã công bố trên thế giới. Các nghiên cứu cho thấy kết quả khả quan về tính an toàn, khả năng dung nạp, đặc biệt giảm tải lượng virus rõ rệt ở bệnh nhân thể nhẹ sau 5 ngày điều trị, giảm tỷ lệ nhập viện, giảm t.ử v.ong;
Đồng thời căn cứ vào kết quả đ.ánh giá giữa kỳ của các nghiên cứu thử nghiệm lâm sàng tiến hành tại Bệnh viện Thống Nhất, Bệnh viện Phổi Trung ương, Đại học Y Dược TP.HCM cho thấy tính an toàn và hiệu quả thuốc, Bộ Y tế đã cho phép triển khai Chương trình sử dụng thuốc có kiểm soát Molnupiravir cho các trường hợp mắc Covid-19 thể nhẹ tại cộng đồng tại TP.HCM từ giữa tháng 8/2021 và hiện nay đã mở rộng triển khai tại 46 địa phương có dịch trong toàn quốc.
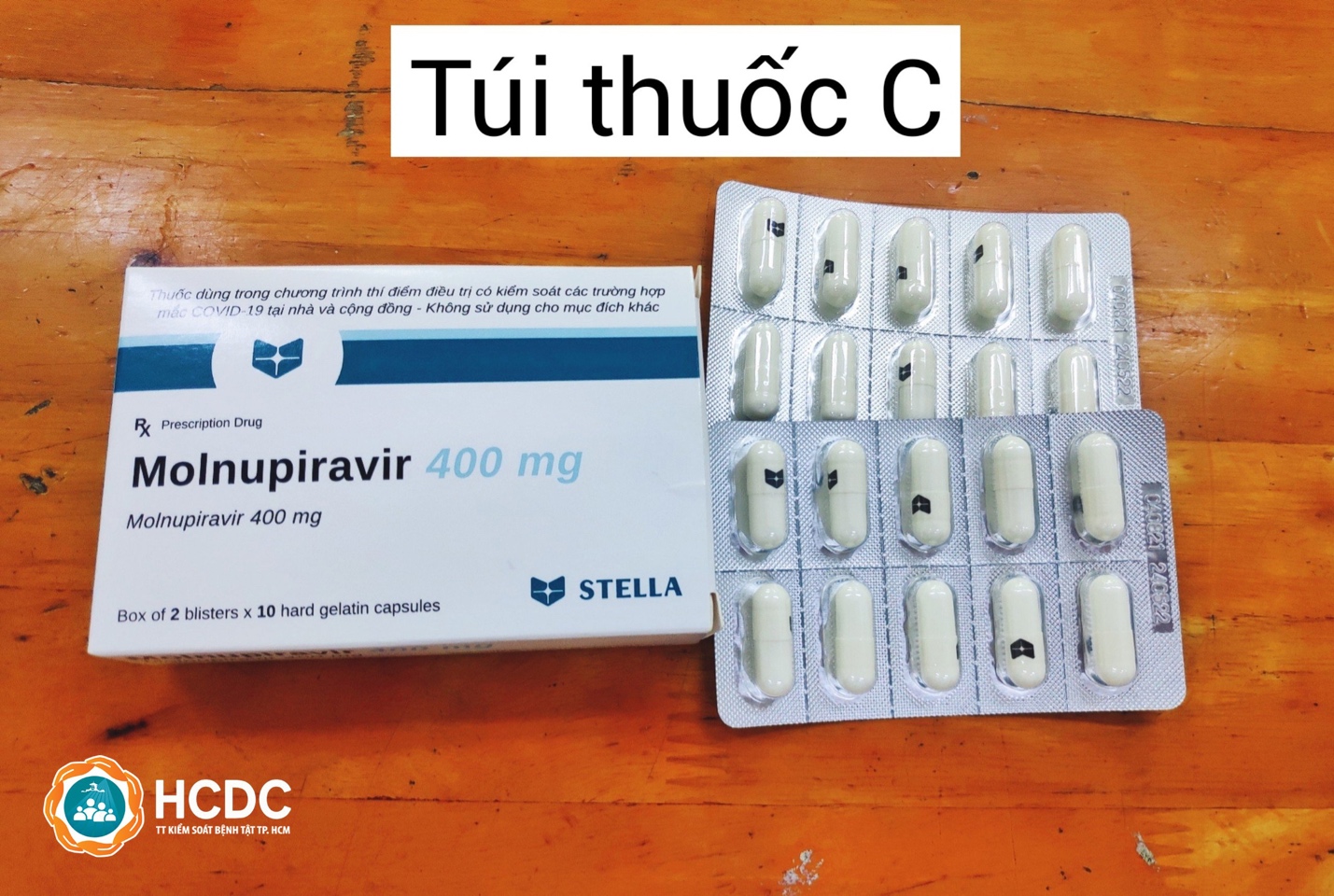
Túi thuốc C hiện nay có thuốc Molnupiravir. Ảnh HCDC
Việc triển khai chương trình tuân thủ các đề cương nghiên cứu khoa học, chặt chẽ đã được Hội đồng đạo đức trong nghiên cứu y sinh học Quốc gia thẩm định, chấp thuận, được Bộ Y tế phê duyệt và được theo dõi, kiểm soát, ghi nhận, đ.ánh giá và tổng kết bởi các chuyên gia, cán bộ, nhân viên y tế.
Thuốc Molnupiravir giảm bệnh nhân Covid-19 chuyển nặng
Theo Bộ Y tế, sau một thời gian sử dụng Molnupiravir, các kết quả báo cáo giữa kỳ của chương trình tại 22 tỉnh/thành phố cho thấy thuốc Molnupiravir có tính an toàn cao, dung nạp tốt, hiệu quả rõ rệt về giảm tải lượng virus, giảm lây lan, giảm chuyển nặng, rút ngắn thời gian điều trị với tỷ lệ bệnh nhân.
Cụ thể, bệnh nhân có kết quả xét nghiệm RT-PCR sau 5 ngày âm tính hoặc dương tính với giá trị CT 30 từ 72,1% đến 99,1%; tỷ lệ bệnh nhân có kết quả xét nghiệm RT-PCR sau 14 ngày âm tính hoặc dương tính với giá trị CT 30 gần 100%; tỷ lệ chuyển nặng rất thấp từ 0,02%-0,06% và không có ca nào dẫn đến t.ử v.ong.
Bộ Y tế cho biết, Molnupiravir là một thuốc kháng virus, hiện chưa được cấp phép lưu hành tại Việt Nam. Hiện cơ quan quản lý dược phẩm và thực phẩm Hoa Kỳ (US-FDA) đang xem xét các dữ liệu lâm sàng cho việc quyết định cấp phép lưu hành thuốc tại Hoa Kỳ.
Tương tự, các quốc gia châu Á trong đó có Ấn Độ cũng đang rà soát các dữ liệu lâm sàng đối với các thuốc được công ty phát minh là MSD nhượng quyền sản xuất cũng như các thuốc chưa được MSD nhượng quyền để xem xét việc cấp giấy đăng ký lưu hành thuốc.

Phát thuốc cho các F0 điều trị tại nhà ở TP.HCM (Ảnh HCDC)
Khuyến cáo tuân thủ chặt các quy định khi cho bệnh nhân Covid-19 dùng thuốc Molnupiravir
Do vậy, việc sử dụng thuốc Molnupiravir hiện nay tại Việt Nam được tiến hành thông qua hình thức nghiên cứu tại cộng đồng trong khuôn khổ Chương trình thí điểm điều trị có kiểm soát chặt chẽ.
Việc triển khai Chương trình cần tuân thủ đề cương nghiên cứu khoa học, chặt chẽ đã được Hội đồng đạo đức trong nghiên cứu y sinh học Quốc gia thẩm định, chấp thuận và được Bộ Y tế phê duyệt.
Việc theo dõi, kiểm soát, ghi nhận, đ.ánh giá bệnh nhân trong Chương trình được tiến hành bởi các chuyên gia, cán bộ, nhân viên y tế theo các tiêu chí an toàn và hiệu quả của đề cương nghiên cứu.
Bên cạnh đó, do thuốc chưa được cấp phép lưu hành rộng rãi nên việc quản lý thuốc nghiên cứu cần phải hết sức chặt chẽ để tránh thất thoát hoặc sử dụng sai mục đích nghiên cứu.
Bộ Y tế sẽ tiếp tục cập nhật các thông tin khoa học của thuốc cũng như tình hình cấp phép sử dụng tại các quốc gia làm cơ sở báo cáo với Chính phủ và các cơ quan chức năng cho phép cấp phép sử dụng khẩn cấp tại Việt Nam trong thời gian sớm nhất.
Bên cạnh đó, để đảm bảo quyền lợi của người dân, Bộ Y tế sẽ tiếp tục hỗ trợ các địa phương có dịch tham gia và triển khai Chương trình trên tinh thần tiếp cận sớm với thuốc Molnupiravir song vẫn phải tuân thủ đề cương nghiên cứu đã được Bộ Y tế phê duyệt và phải kiểm soát, theo dõi chặt chẽ các tiêu chí an toàn, hiệu quả cũng như quản lý thuốc nghiên cứu để bảo đảm an toàn cho các bệnh nhân tham gia Chương trình.
